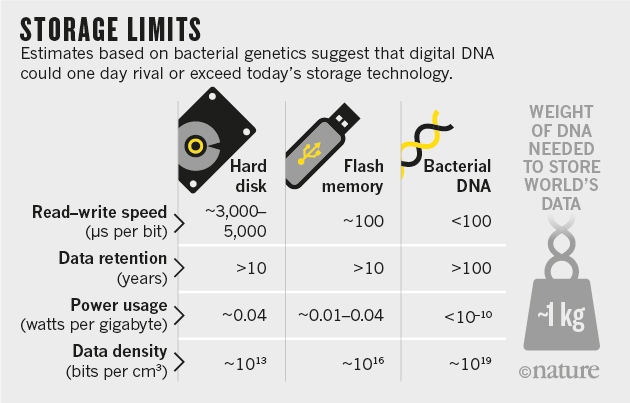
nrg έγραψε:Sarastro έγραψε:Αυθαίρετος συλλογισμός. Προφανώς τα αμινοξέα έχουν διαφορετικές χημικές ιδιότητες που κάνουν κάποιους συνδυασμούς αδύνατους. Δεν υπάρχει κανένας λόγος να υποθέσει κανείς ότι θα δοκιμάζονταν τυχαία όλοι οι συνδυασμοί.
Δεν χρειάζεται να αρνηθείς έναν "αυθαίρετο συλλογισμό", παρουσιάζοντας ένα ακόμα πιο αυθαίρετο επιχείρημα. Αν υπάρχουν περιορισμοί μεταξύ του τρόπου, με το οποίο ενώνονται τα αμινοξέα, απλά μας τον παρουσιάζεις.
Αγαπάμε την επιστήμη, σωστά;
Ομοίως, αν έχουμε σε έναν χώρο υδρογόνο και οξυγόνο και βάλουμε φωτιά, θα προκύψει αμέσως νερό, ακόμη και αν υπάρχουν στον ίδιο χώρο και όλα τα άλλα χημικά στοιχεία. Δεν θα αρχίσουν να γίνονται όλοι οι συνδυασμοί.
Σου απάντησα παραπάνω. Το ξέχασες;
viewtopic.php?f=23&t=7422&start=570#p174009
Oταν όλο σου το επιχείρημα βασίζεται στο ότι είναι αδύνατη η αβιογένεση γιατί γιά τον σχηματισμό των πρωτεϊνών δεν φθάνει όλη η διάρκεια ζωής του Σύμπαντος, αφού όλοι οι συνδυασμοί είναι εξ ίσου πιθανοί, το ελάχιστο που μπορεί να περιμένει κανείς, είναι να μπορείς να υποστηρίξεις αυτό τον τελευταίο ισχυρισμό, ότι δηλαδή όλοι οι συνδυασμοί είναι εξ'ίσου πιθανόν να συμβούν. Και αυτή η υποστήριξη θα έπρεπε να είναι κάτι καλύτερο από το "και γιατί να μην είναι" που προτάσεις εσύ.
Ας είναι κι'έτσι όμως. Γιά να δούμε αν υπάρχουν περιορισμοί στον τρόπο με τον οποίο ενώνονται τα αμινοξέα:
https://en.wikipedia.org/wiki/Proteinogenic_amino_acidΕκεί μέσα βλέπουμε διάφορα:
- O χημικός τύπος των αμινοξέων είναι εντελώς διαφορετικός. Δύο από αυτά περιέχουν θείο και ένα σελήνιο.
- Το μοριακό βάρος του μεγαλύτερου προς το μικρότερο είναι τής τάξης του 3,40 που δεν το λες και αμελητέο.
- Το ισοηλεκτικό τους σημείο (δηλαδή το pH όπου το ηλεκτρικό φορτίο είναι ουδέτερο) κυμαίνεται από 3,15 έως 10,76
- Κάποια από αυτά έχουν υδρόφιλο μέρος, ενώ άλλα δεν έχουν.
Μετά από αυτά, κάποιος θα είχε δυσκολίες να υποστηρίξει πως όλα μπορούν να ανταλλαγούν αδιάκριτα στις χημικές αντιδράσεις. Aλλά δεν μένουμε μόνο εκεί. Στις ιδιότητες αναφέρονται μεταξύ άλλων, τα εξής:
- Asp behaves similarly to glutamic acid, and carries a hydrophilic acidic group with strong negative charge. Usually, it is located on the outer surface of the protein, making it water-soluble. It binds to positively charged molecules and ions, and is often used in enzymes to fix the metal ion. When located inside of the protein,
aspartate and glutamate are usually paired with arginine and lysine.
- Lys is essential for humans, and behaves similarly to arginine. It contains a long, flexible side chain with a positively charged end. The flexibility of the chain makes lysine and arginine suitable for binding to molecules with many negative charges on their surfaces. E.g., DNA-binding proteins have their active regions rich with arginine and lysine.
The strong charge makes these two amino acids prone to be located on the outer hydrophilic surfaces of the proteins; when they are found inside, they are usually paired with a corresponding negatively charged amino acid, e.g., aspartate or glutamate.
Τέλος, αφήνω εδώ και το παρακάτω διάγραμμα, που υποθέτω ότι υποστηρίζει το γεγονός τής ανταλλαξιμότητας όλων ανεξαρτήτως των αμινοξέων

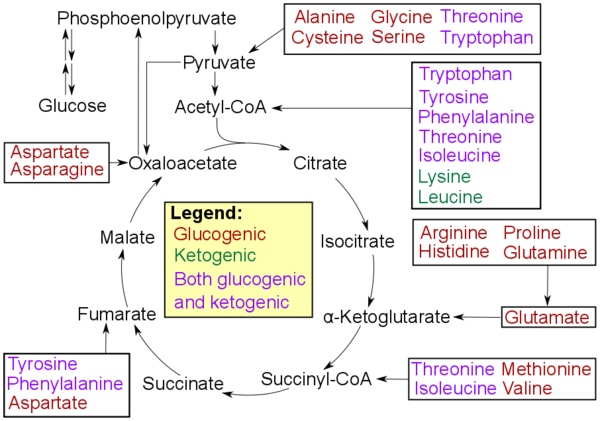
.gif)

 )
)